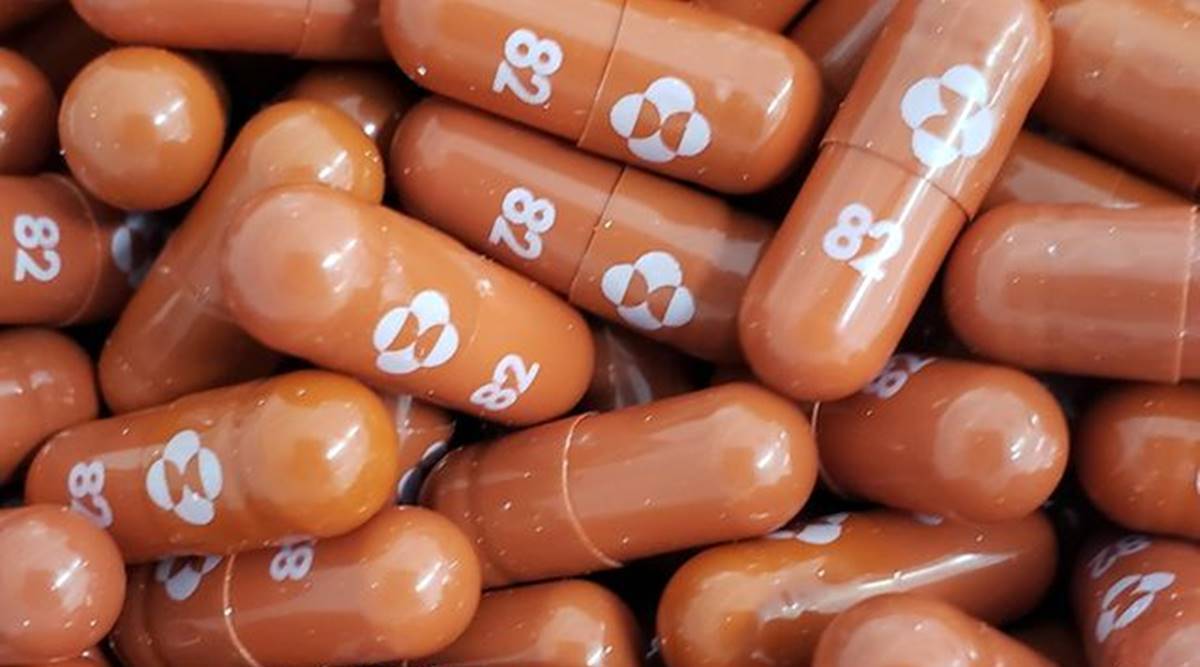
El fármaco oral experimental de Merck & Co Inc para COVID-19, molnupiravir, redujo en alrededor de un 50% la posibilidad de hospitalización o muerte de pacientes con riesgo de enfermedad grave, según los resultados de los ensayos clínicos provisionales anunciados el viernes.
Merck y su socio Ridgeback Biotherapeutics planean solicitar la autorización de uso de emergencia para la píldora en EE. UU. Lo antes posible y enviar solicitudes a las agencias reguladoras de todo el mundo.
Hoy anunciamos datos provisionales positivos para nuestra investigación. #COVID-19 #antivírico tratamiento. Obtenga más información sobre nuestras últimas noticias: https://t.co/v1DDAa4RjN $ MRK pic.twitter.com/na2O4Y5N3D
– Merck (@Merck) 1 de octubre de 2021
Debido a los resultados positivos, el ensayo de fase 3 se interrumpirá antes de tiempo por recomendación de monitores externos. «Esto va a cambiar el diálogo sobre cómo administrar COVID-19», dijo Robert Davis, director ejecutivo de Merck. Reuters.
Si se autoriza, molnupiravir, que está diseñado para introducir errores en el código genético del virus, sería el primer medicamento antiviral oral para COVID-19. Rivales como Pfizer Inc y la farmacéutica suiza Roche Holding AG están compitiendo para desarrollar una píldora antiviral fácil de administrar para COVID-19, pero hasta ahora, solo los cócteles de anticuerpos, que deben administrarse por vía intravenosa, están aprobados para tratar el COVID no hospitalizado. 19 pacientes.
Un análisis intermedio planificado de 775 pacientes en el estudio de Merck encontró que el 7,3 por ciento de los que recibieron molnupiravir fueron hospitalizados o habían muerto 29 días después del tratamiento, en comparación con el 14,1 por ciento de los pacientes que recibieron placebo. No hubo muertes en el grupo de molnupiravir, pero hubo ocho muertes de pacientes con placebo.
«Los tratamientos antivirales que se pueden tomar en casa para mantener a las personas con COVID-19 fuera del hospital son muy necesarios», dijo Wendy Holman, directora ejecutiva de Ridgeback, en un comunicado.
En el ensayo, que incluyó a pacientes de todo el mundo, se tomó molnupiravir cada 12 horas durante cinco días. El estudio incluyó a pacientes con COVID-19 leve a moderado confirmado por laboratorio, que presentaban síntomas durante no más de cinco días. Todos los pacientes tenían al menos un factor de riesgo asociado con una mala evolución de la enfermedad, como la obesidad o la edad avanzada.
Merck dijo que la secuenciación viral realizada hasta ahora muestra que el molnupiravir es eficaz contra todas las variantes del coronavirus, incluida la altamente transmisible Delta. La compañía dijo que las tasas de eventos adversos fueron similares para los pacientes con molnupiravir y placebo, pero no dio detalles de los efectos secundarios.
Merck ha dicho que los datos muestran que el molnupiravir no es capaz de inducir cambios genéticos en las células humanas, pero los hombres inscritos en sus ensayos deben abstenerse de tener relaciones heterosexuales o aceptar utilizar métodos anticonceptivos. Las mujeres en edad fértil no pueden estar embarazadas y también deben usar métodos anticonceptivos.
Merck dijo que espera producir 10 millones de ciclos del tratamiento para fines de 2021, y el próximo año se recibirán más dosis. La compañía tiene un contrato con el gobierno de EE. UU. Para suministrar 1,7 millones de cursos de molnupiravir a un precio de $ 700 por curso.
El CEO Davis dijo que Merck tiene acuerdos similares con otros gobiernos en todo el mundo y está en conversaciones con más. La compañía dijo que planea implementar un enfoque de precios escalonados basado en los criterios de ingresos del país. Merck también acordó licenciar el medicamento a varios fabricantes de medicamentos genéricos con sede en India, que podrían suministrar el tratamiento a países de ingresos bajos y medios.
El molnupiravir también se está estudiando en un ensayo de fase 3 para prevenir la infección por coronavirus en personas expuestas al virus. Los funcionarios de Merck dijeron que no está claro cuánto tiempo llevará la revisión del medicamento por parte de la FDA. «Creo que van a intentar trabajar con prontitud en esto», dijo Dean Li, director de los laboratorios de investigación de Merck.