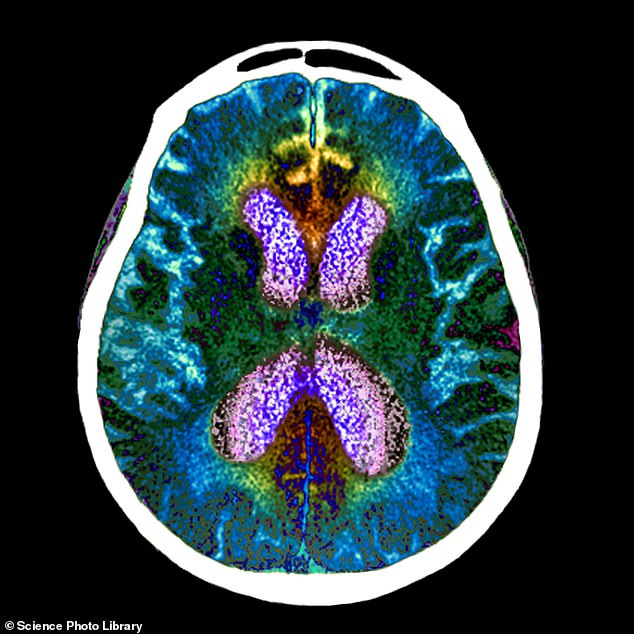
Un fármaco experimental para el Alzheimer desarrollado por Eisai Co Ltd y Biogen Inc redujo significativamente el deterioro cognitivo y funcional en un gran ensayo de pacientes en las primeras etapas de la enfermedad, dijeron las compañías el martes.
El fármaco inyectado, lecanemab, ralentizó el progreso de la enfermedad de desgaste cerebral en un 27 por ciento en comparación con un placebo, lo que cumplió con el objetivo principal del estudio y ofreció una aparente victoria para las empresas y, potencialmente, para los pacientes y sus familias desesperados por un tratamiento eficaz.
Eisai dijo que los resultados del ensayo de 1.800 pacientes prueban la teoría de larga data de que la eliminación de los depósitos pegajosos de una proteína llamada beta amiloide del cerebro de las personas con Alzheimer temprano puede retrasar el avance de la enfermedad debilitante.
Analistas, como Salim Syed de Mizuho Securities, han dicho que los resultados se considerarían una «victoria» si lecanemab redujera la tasa de caída en alrededor de un 25 por ciento, y que las acciones de ambas compañías podrían aumentar con la noticia.
Lecanemab, al igual que el fármaco anterior Aduhelm de las empresas, es un anticuerpo diseñado para eliminar esos depósitos de amiloide.
A diferencia de Aduhelm, lecanemab se dirige a formas de amiloide que aún no se han agrupado.
Un fármaco experimental para la enfermedad de Alzheimer, llamado lecanemab, ha disminuido significativamente el deterioro cognitivo y funcional en un 27 % en un gran ensayo con pacientes

Los analistas, como Salim Syed (en la foto) de Mizuho Securities, dicen que una disminución del 25 por ciento sería una «ganancia»

Los resultados de un ensayo de 1800 pacientes demostraron la teoría de que la eliminación de los depósitos pegajosos de proteína llamada beta amiloide puede retrasar la enfermedad debilitante

La enfermedad de Alzheimer es una enfermedad progresiva y degenerativa del cerebro, en la que la acumulación de proteínas anormales provoca la muerte de las células nerviosas.
Algunos científicos han cuestionado la llamada hipótesis amiloide, particularmente después de la controvertida aprobación de Aduhelm por parte de la Administración de Drogas y Alimentos de los EE.
La decisión se tomó después de que el propio panel de expertos externos de la FDA desaconsejara la aprobación.
Aduhelm fue el primer fármaco nuevo para el Alzheimer aprobado en 20 años después de una larga lista de fallas de alto perfil para la industria.
Eisai, líder del programa de lecanemab de la asociación 50-50, está buscando la aprobación de la FDA bajo la misma vía acelerada que Aduhelm, y se espera una decisión a principios de enero.
Pero el martes, el fabricante de medicamentos japonés dijo que usará los nuevos resultados de eficacia para enviar lecanemab a la revisión tradicional de la FDA.
La compañía dijo que también buscará autorización en Japón y Europa durante su actual año fiscal, que finaliza el 31 de marzo.
El ensayo de Fase III evaluó la capacidad del fármaco para reducir el deterioro cognitivo y funcional según la Clinical Dementia Rating-Sum of Boxes (CDR-SB), una escala numérica utilizada para cuantificar la gravedad de la demencia en pacientes en áreas como la memoria, la orientación, la juicio y resolución de problemas y cuidado personal.
La tasa de ARIA-E, un efecto secundario de inflamación cerebral asociado con los tratamientos antiamiloides, fue del 12,5 por ciento en el grupo de lecanemab, frente al 1,7 por ciento en el grupo de placebo.
Si bien el efecto secundario apareció en las imágenes, muchos de estos casos no fueron sintomáticos, dijeron las compañías.
Se observó inflamación cerebral sintomática en el 2.8 por ciento de los del grupo de lecanemab y en ninguno del grupo de placebo, dijeron.
El medicamento, lecanemab, está siendo desarrollado por Biogen y Eisai, las mismas dos compañías farmacéuticas detrás de Aduhelm.

Eisai, líder del programa de lecanemab de la asociación 50-50, está buscando la aprobación de la FDA bajo la misma vía acelerada que Aduhelm, y se espera una decisión a principios de enero.
Se observó inflamación cerebral sintomática en el 2.8 por ciento de los del grupo de lecanemab y en ninguno del grupo de placebo
El ensayo también rastreó la tasa de microhemorragias en el cerebro, que ocurrieron a una tasa del 17 por ciento en el grupo de lecanemab y del 8,7 por ciento en el grupo de placebo.
La incidencia total de ambas afecciones fue del 21,3 por ciento en el grupo de lecanemab y del 9,3 por ciento en el grupo de placebo, tasas que se ubicaron dentro del rango esperado, dijeron las compañías.
La aprobación de Aduhelm fue un punto brillante poco común para los pacientes de Alzheimer, pero los críticos han pedido más evidencia de que los medicamentos dirigidos contra el amiloide valen la pena.
La controversia y la renuencia de algunos pagadores a cubrir Aduhelm llevaron a Biogen a reducir el precio del medicamento a $28,000 por año desde los $56,000 iniciales.
Pero Medicare, el plan de salud del gobierno de EE. UU. para personas mayores de 65 años, dijo este año que solo pagaría Aduhelm si los pacientes se inscribían en un ensayo clínico válido, lo que restringió drásticamente el uso del medicamento.
Dado que el Alzheimer es una enfermedad del envejecimiento, aproximadamente el 85 por ciento de los pacientes elegibles para el medicamento están cubiertos por el plan del gobierno.
Se espera que la cantidad de estadounidenses que viven con Alzheimer aumente a alrededor de 13 millones para 2050 desde los más de 6 millones actuales, según la Asociación de Alzheimer.
A nivel mundial, esa cifra podría aumentar a 139 millones para 2050 sin un tratamiento eficaz, según Alzheimer’s Disease International.
Otros anticuerpos dirigidos a la placa en la última etapa de desarrollo para pacientes con Alzheimer incluyen el gantenerumab de Roche Holding AG y el donanemab de Eli Lilly and Co.